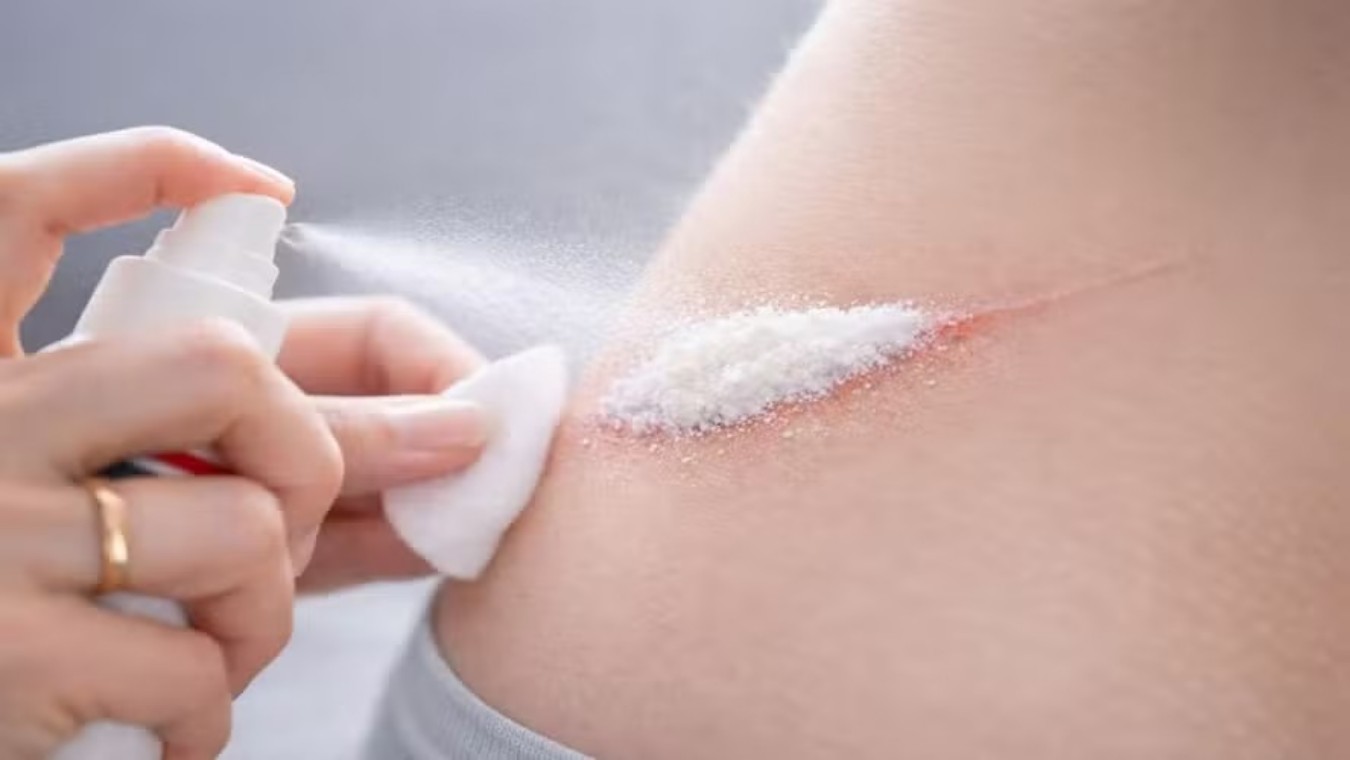
Pesquisadores criam spray capaz de estancar hemorragias em segundos
| 599 viewsUm ferimento grave pode levar à morte em poucos minutos quando o sangramento não é controlado a tempo. É esse intervalo crítico que uma equipe de cientistas sul-coreanos tenta reduzir com uma nova tecnologia: um pó em spray capaz de estancar hemorragias quase imediatamente.