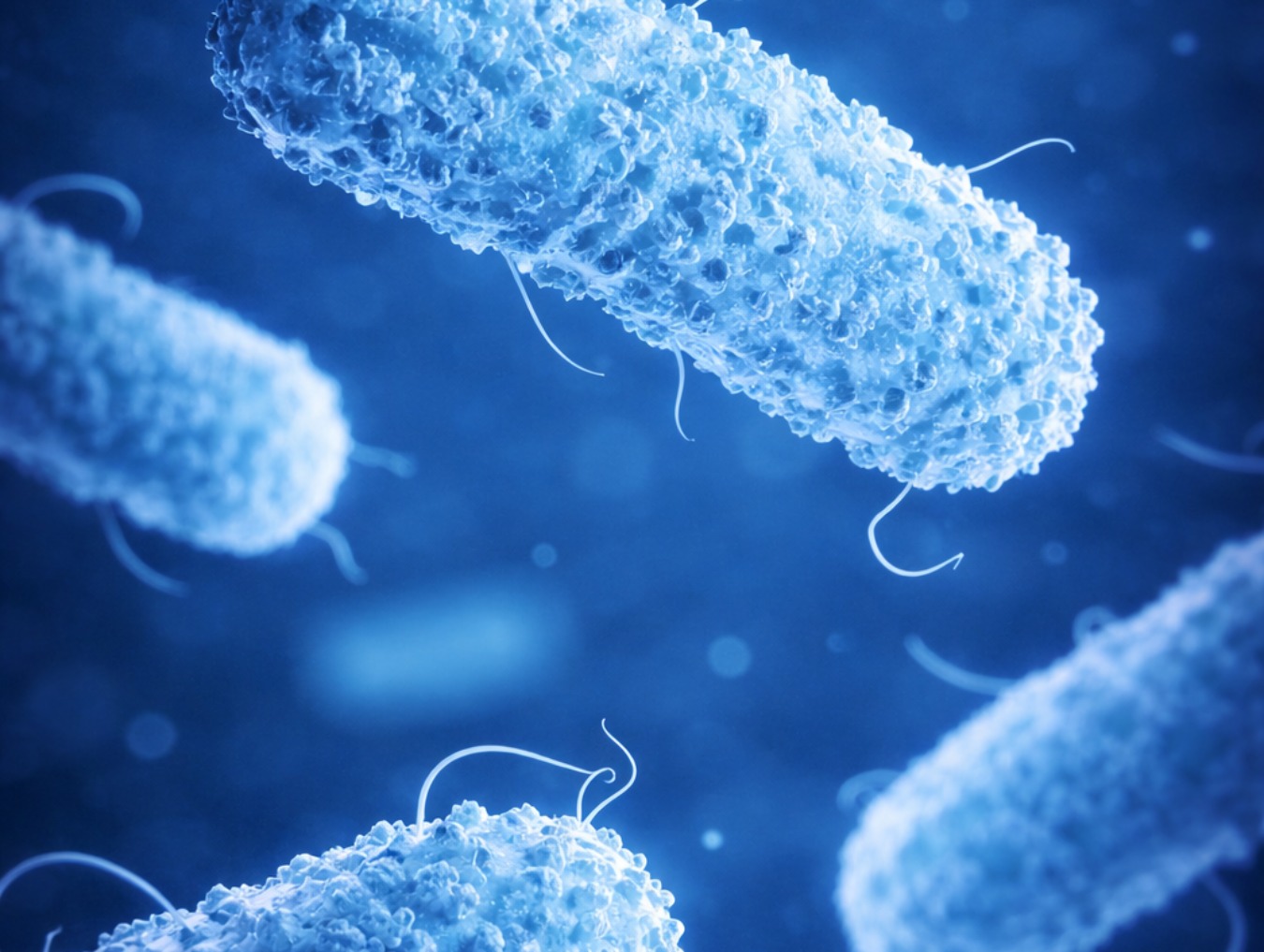
Hidrogel brasileiro mostra ação contra superbactérias e aponta novos caminhos para controle de infecções hospitalares
| 524 viewsO avanço das superbactérias tem levado a ciência a buscar alternativas além dos antibióticos tradicionais. Um estudo recente, desenvolvido por pesquisadores da Universidade Tecnológica Federal do Paraná e publicado na revista científica Science Direct, apresenta uma dessas possibilidades: um hidrogel com elevado poder antimicrobiano, capaz de atuar contra microrganismos resistentes e aumentar a segurança em ambientes hospitalares.