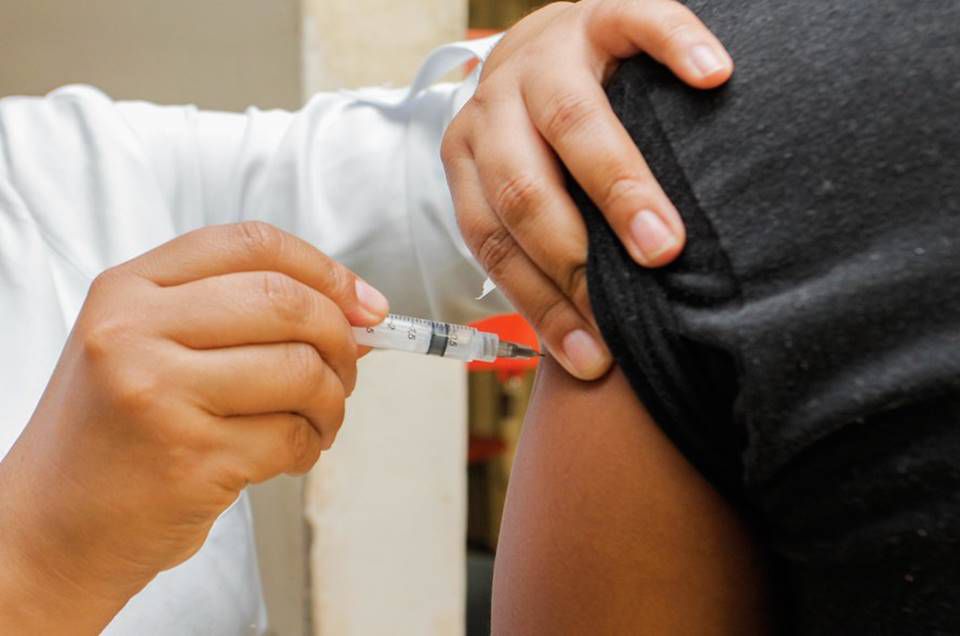
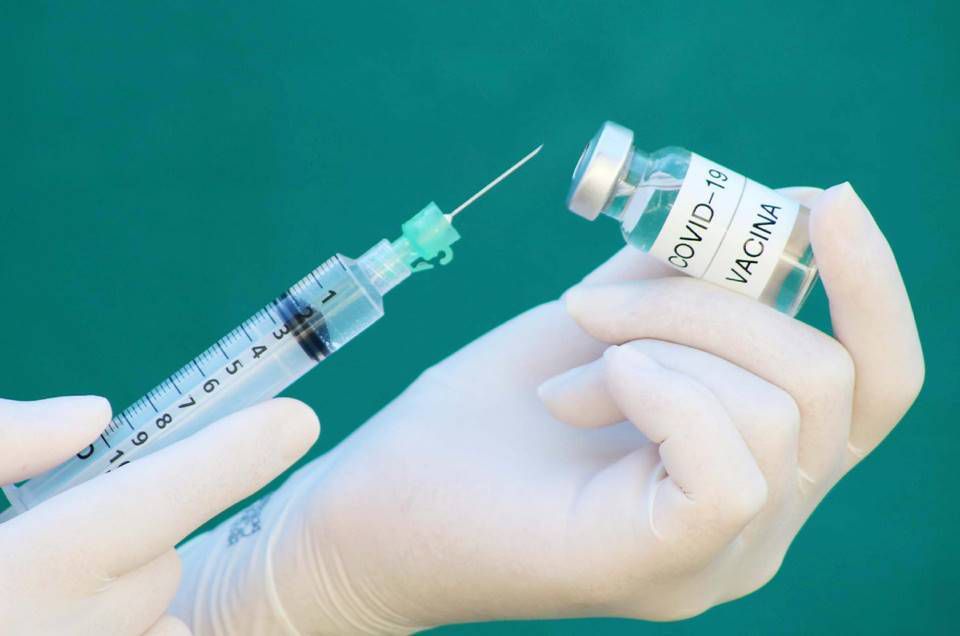
O Governo de São Paulo entregou à Agência Nacional de Vigilância Sanitária (Anvisa) a documentação sobre a vacina coronavac, que é uma parceria do Instituto Butantan com a chinesa Sinovac, para o registro do imunizante. A vacina está na fase 3 de testes no Brasil, aquela realizada em humanos, informou o Estadão.
De acordo com o governo paulista, o Butantan enviou à Anvisa uma avaliação de dados preliminares de produtos biológicos para Covid-19 e os relatórios de segurança e eficácia obtidos com a coronavac em testes não-clínicos, ou seja, feitos em laboratório ou em animais antes da testagem em humanos.
O governador de São Paulo João Doria confirmou na sexta-feira (2/10) que o governo registrou, um dia antes, no órgão regulador a documentação da coronavac para análise e obtenção do registro. “A Anvisa recebeu as informações por meio de uma plataforma digital. Esses documentos já foram enviados pelo Instituto Butantã para registro da vacina contra o coronavírus. Nosso objetivo é tornar esse processo mais rápido, mas sempre dentro das normas científicas, seguindo todos os protocolos”, salientou Doria, segundo o Estadão.
Para os casos das vacinas contra a Covid-19, a Anvisa criou um novo procedimento regulatório, chamado de submissão contínua. Ele foi elaborado pela Agência visando dar maior agilidade à análise devido à urgência imposta pela pandemia. Com a simplificação, não será mais preciso esperar que todos os dados e documentos técnicos estejam disponíveis, nem que sejam preenchidos os requerimentos regulatórios necessários ao pedido de registro.
A Anvisa analisa os dados na medida em que eles chegam, “até que evidências suficientes estejam disponíveis para suportar um pedido formal de registro”. A área técnica do órgão está avaliando também o primeiro conjunto de informações sobre a vacina desenvolvida pela AstraZeneca em parceria com a Universidade de Oxford, informou o site Poder 360.
Conforme o diretor do Instituto Butantan, Dimas Tadeu Covas, a nova normativa da Anvisa facilita o fluxo de documentos para registro de vacinas para o coronavírus. “Foi estabelecido um fluxo contínuo e os documentos podem ser remetidos à medida que são gerados. Isso tem o objetivo de facilitar a análise dos técnicos, para que não tenha atraso nesse processo tão importante. Já submetemos os documentos disponíveis da nossa vacina à Anvisa. Isso mostra o comprometimento de que estudos de registro da vacina sejam feitos rapidamente”, declarou Covas ao Estadão.
No dia 30 de setembro, o governo de São Paulo assinou contrato com a Sinovac de fornecimento de 46 milhões de doses da coronavac até dezembro deste ano. Nesse período, a farmacêutica vai enviar 6 milhões de doses da vacina já prontas, enquanto outras 40 milhões serão formuladas e envasadas em São Paulo. Outras 14 milhões de doses devem ser fornecidas até fevereiro do ano que vem, mas isso ainda não está fechado.
Ao anunciar a assinatura do contrato à imprensa, Doria afirmou que, se a coronavac passar na fase de testes em voluntários e for aprovada pela Anvisa, a vacinação poderá ocorrer a partir de 15 dezembro e começará em profissionais de saúde de unidades públicas e privadas de saúde de São Paulo.
Receba nossas notícias por e-mail: Cadastre aqui seu endereço eletrônico para receber nossas matérias diariamente
O secretário estadual da Saúde, Jean Gorinchteyn, lembrou que o processo está mais ágil. “Os procedimentos antes demoravam até um ano, mas no que tange à Covid-19 foi estreitado para 60 dias. Com isso, muito possivelmente teremos esse registro no final de novembro, início de dezembro. O começo da vacinação se dará após essa autorização”.
Desde julho a coronavac vem sendo testada no Brasil. Atualmente, os estudos clínicos em voluntários acontecem em 12 centros de pesquisa em cinco Estados e no Distrito Federal. O estudo da vacina foi ainda ampliado no País, passando de nove mil para 13 mil voluntários. Tanto na China quanto no Brasil, os testes clínicos passaram a envolver voluntários com mais de 60 anos. A expectativa é de que todos os voluntários sejam vacinados neste mês.
Segundo o governo paulista, estudo feito em 50 mil pessoas na China indicou segurança da coronavac. De acordo com as informações, 94,7% dos voluntários não apresentaram qualquer efeito adverso – índice que se equipararia a outras vacinas já amplamente usadas no Brasil, como a da gripe. Mas os testes continuam e somente a partir de 15 de outubro que será possível começar a ter informações sobre a eficácia do imunizante em humanos, conforme o Estadão.
Participe também: Grupo de WhatsApp e telegram para receber notícias farmacêuticas diariamente
Obrigado por apoiar o jornalismo profissional
A missão da Agência de notícias do ICTQ é levar informação confiável e relevante para ajudar os leitores a compreender melhor o universo farmacêutico. O leitor tem acesso ilimitado às reportagens, artigos, fotos, vídeos e áudios publicados e produzidos, de forma independente, pela redação da Instituição. Sua reprodução é permitida, desde que citada a fonte. O ICTQ é o principal responsável pela especialização farmacêutica no Brasil. Muito obrigado por escolher a Instituição para se informar.