Uma nova safra de drogas que promete avanços reacende debates sobre melhor forma de tratamento da doença
Nala tinha 55 anos quando começou a ter dificuldades no trabalho. Ela desenvolveu uma demência progressiva. Exames genéticos e testes feitos a partir de imagens do cérebro apontavam para uma direção - o diagnóstico de Alzheimer. Com o tempo - pouco tempo - Nala tornou-se incapaz de vestir-se, tomar banho, pentear o cabelo ou ir ao banheiro sozinha. Em suma, não conseguia executar tarefas entre as mais corriqueiras. Ainda assim, conservou intacta sua capacidade de tocar piano maravilhosamente.
Esse caso, ao mesmo tempo intrigante e devastador, é descrito nesses termos pelo médico americano Dale Bredesen no livro “O fim do Alzheimer”. A história de Nala esboça, ainda que em grandes traços, as principais características da doença. Peculiaridades, aliás, que a tornam uma das mais assustadoras que existem. Das famílias, além da dor permanente, exige cuidados tão intensos quanto dispendiosos (os custos globais superam a casa do US$ 1 trilhão por ano). Nos pacientes, ela mata a memória - e com isso dissipa todo um acervo de laços afetivos -, antes mesmo de pôr fim à vida.
Trata-se de um roteiro com uma carga dramática tão contundente que não poderia deixar de ser espelhada - e explorada - em criações de toda a sorte, caso de filmes como “Meu Pai” (Oscar de melhor ator para Anthony Hopkins, em 2021), “Para Sempre Alice” (Oscar de melhor atriz para Julianne Moore, em 2015), ou mesmo “Longe Dela”, de 2006, um clássico desse filão temático, com Julie Christie (a musa de “Doutor Jivago”) e Gordon Pinsent, que não rendeu o Oscar a ninguém, mas foi muito elogiado pela crítica.
Não por acaso, qualquer fato novo que traga à cena a palavra Alzheimer ecoa pesadamente. E foi isso o que aconteceu no mês passado. Após um ano de análise, a Anvisa negou o registro no Brasil de um novo medicamento contra a doença, o aducanumabe, cujo nome comercial nos Estados Unidos é Aduhelm, produzido pelos laboratórios Biogen, americano, e Eisai, japonês.
As empresas informaram que ainda analisam o que farão. Podem recorrer da decisão, mas não será tarefa simples revertê-la. “A recusa do medicamento não só era esperada como desejada”, diz o neurologista Ricardo Nitrini, da Universidade de São Paulo (USP). O médico foi um dos mentores de uma carta produzida pela Academia Brasileira de Neurologia (ABN) contra a aprovação do medicamento no país. Há, contudo, quem discorde. “Drogas como essa deveriam ter seu espaço, ter uma oportunidade no Brasil”, opina o neurologista Rodrigo Schultz, presidente da Associação Brasileira de Alzheimer (ABRAz), entidade que reúne parentes e cuidadores de pacientes.
Tem sido assim no mundo inteiro. Há um racha entre os que contestam e os que aprovam o uso do remédio, ainda que a balança penda para o primeiro grupo. E o motivo dessa divisão está embutido na própria história do aducanumabe. Ele foi aprovado para uso entre americanos em junho do ano passado, pela Food and Drug Administration (FDA), a agência reguladora do governo americano. O aval, porém, não poderia ter gerado maiores polêmicas.
Os ensaios do medicamento em pessoas começaram em 2011. A fase 3 dos testes, a última antes da aprovação final, teve início em 2015, com dois grandes grupos. Um deles, o “Engage”, reuniu 1.653 pacientes, e o outro, o “Emerge”, mobilizou 1.643 pessoas. No ano seguinte, 2016, um artigo de capa publicado na revista “Nature” trazia resultados espetaculares alcançados pela droga. “Ela passou a ser vista com grande euforia, como se fosse a salvação da lavoura”, diz Schultz, da ABRAz.
Não à toa. Um novo remédio contra o Alzheimer não era aprovado pela FDA havia 19 anos. Todos os medicamentos existentes ajudavam a diminuir os sintomas em algumas situações, mas faziam isso por tempo limitado. A pesquisa nesse setor estava encalhada num deserto de terapias. Para se dar uma ideia da aridez vigente, basta dizer que 244 drogas foram experimentadas entre 2000 e 2010, mas somente uma, a memantina, foi aprovada, em 2003.
Em março de 2019, entretanto, os problemas começaram. A Biogen e a Eisai anunciaram que iriam interromper os testes, pois as provas realizadas não haviam passado pela “análise de futilidade”. Em miúdos, isso queria dizer que os resultados obtidos não justificavam a continuidade dos estudos, levando-se em conta os riscos que implicavam por causa de efeitos colaterais. Ocorre que, em outubro do mesmo ano, houve nova reviravolta e as empresas retomaram o processo de aprovação na FDA.
Aí, formou-se o bafafá. Uma comissão de 11 conselheiros da FDA posicionou-se contra a aprovação da droga. A mídia questionou as relações entre executivos da indústria farmacêutica e a agência reguladora e houve uma grita contra o preço do medicamento, então fixado em US$ 56 mil por ano por paciente, mas reduzido pela metade em janeiro deste ano. Isso para oferecer um resumo da controvérsia.
Para Nitrini, da USP, o aducanumabe iria engrossar a fila da chamada “judicialização da saúde” no Brasil, em que as pessoas recorrem à Justiça para garantir que o SUS banque a compra de medicamentos. “Num país onde os pacientes com Alzheimer e seus familiares não recebem nada, não contam com quase nada, me parece um erro gastar um dinheirão com um remédio cujo efeito ainda precisa ser demonstrado com maior clareza”, diz. “Meu problema em relação a esse assunto não é como médico; é como cidadão.” Schultz, da ABRAz, rebate: “Apesar das dificuldades do país, que são reais, drogas como essa deveriam ter uma oportunidade”.
A Biogen informa que confia nos dados clínicos obtidos nos exames. A empresa aponta que, num primeiro momento, houve um desbalanço estatístico na análise dos testes de fase 3. Uma verificação posterior mostrou que num dos estudos, o “Emerge”, os pacientes submetidos por mais tempo à dose máxima do aducanumabe (10 miligramas por quilo de peso) registraram melhoras clínicas substanciais.
Houve, segundo a indústria, uma redução de 22% no declínio das funções cognitivas (memória, orientação e linguagem), uma diminuição de 40% do comprometimento das atividades rotineiras (fazer compras, comer e até tomar banho), além de uma queda de 87% em sintomas comportamentais (agressividade e ansiedade). Como condição de manter o aval da droga, porém, a FDA exigiu a realização de novos testes, numa espécie de tira-teima, num prazo de até nove anos. A Biogen acredita que poderá concluí-los em quatro ou cinco anos.
Receba nossas notícias por e-mail: Cadastre aqui seu endereço eletrônico para receber nossas matérias
Toda essa polêmica não é mais do que um “esquenta” em se tratando do que vem por aí. O aducanumabe, como modelo de terapia, não é um fato isolado. Ele representa uma ninhada de drogas que está prestes a desabar no colo das agências regulatórias para conquistar o mercado. A maior parte delas está calcada numa só teoria. Trata-se da “cascata amiloide”. A tese, que vem ganhando força desde os anos 1980, indica que a principal fonte do Alzheimer está em alterações provocadas pelo acúmulo de duas proteínas, que comprometem o funcionamento dos neurônios. Para entender esse processo, vale a pena fazer um breve mergulho no órgão mais complexo do corpo humano.
Um cérebro adulto saudável tem perto de 100 bilhões de neurônios, as células responsáveis pela transmissão de impulsos nervosos. Como observa o médico americano Dale Bredesen, cada neurônio tem uma média de 10 mil conexões, para quase 1 quatrilhão (isso é 1.000.000.000.000) de conexões totais, ou sinapses. E é ótimo que sejam tantas e tão pródigas, pois permitem que os sinais viajem velozmente pelo cocuruto e as informações por elas conduzidas criem a base celular de memórias, pensamentos, sensações, emoções, movimentos e habilidades. Aliás, sem esse mecanismo gigante as letras desse texto não passariam de um amontoado de manchinhas pretas sem sentido à sua frente.
Pois, em 1906, o psiquiatra e neuropatologista alemão Alois Alzheimer identificou duas alterações - lesões - no cérebro de Auguste Deter, uma mulher de 55 anos. Ela havia sido internada cinco anos antes, aos 50 anos, com um quadro de demência, num hospital para doentes mentais e epilépticos de Frankfurt, na Alemanha. O local era conhecido como o “Castelo dos Insanos”. Pouco tempo depois, as mesmas peculiaridades foram observadas pelo médico tcheco Oskar Fischer, mas em circunstâncias e local diferentes.
O impressionante é que, hoje, 116 anos depois da autópsia, as lesões percebidas por Alzheimer ainda são tidas como duas possíveis grandes vilãs da enfermidade. A primeira ocorre fora dos neurônios com o acúmulo de fragmentos da proteína beta-amiloide, em placas insolúveis, como pedras. O segundo problema decorre da concentração de outra proteína, chamada tau, que forma emaranhados dentro dos neurônios.
Acredita-se que as placas e acúmulos menores de beta-amiloide, chamados oligômeros, contribuem com a morte de neurônios (a neurodegeneração). Os emaranhados de tau bloqueariam o transporte de nutrientes, também comprometendo a sobrevivência dos neurônios.
A tarefa que as novas drogas se propõem a executar, assim como o aducanumabe, é remover placas e novelos formados pelas vilãs. “A questão é até que ponto essa limpeza realmente altera o estado clínico dos pacientes”, diz o neurologista Paulo Bertolucci, da Universidade Federal de São Paulo (Unifesp). “Ninguém trata para melhorar os marcadores [as placas ou os emaranhados]. Nós tratamos para melhorar a vida das pessoas.”
E a fila é grande para participar desse tira-teima. Só a Biogen tem mais três drogas desse tipo no pipeline. São elas o lecanemabe, também criado em parceria com a Eisai, que está na fase final de ensaios clínicos e ataca as placas beta-amiloides. Outras duas, com nomes que parecem códigos, são a BIIB080, desenvolvida em colaboração com a Ionis Pharmaceuticals, uma empresa californiana de biotecnologia, e a BIIB076. Ambas têm como alvo os emaranhados tau e estão em fase inicial de testes.
Entre os gigantes do setor, a Roche trabalha com mais quatro medicamentos dessa espécie. O gantenerumabe, também contra placas, está em estágio mais avançado. Ele recebeu a designação de terapia inovadora da FDA em outubro de 2021. Estudos clínicos estão sendo feitos com cerca de 2 mil pacientes em 350 centros médicos de mais de 30 países. “Se positivos, os achados permitirão buscar a aprovação para o gantenerumabe de autoridades regulatórias de todo o mundo”, informou a empresa. Os testes devem ser concluídos no fim deste ano.
Nitrini, da USP, observa que tem especial interesse nos resultados obtidos pelos anticorpos que atuam nos emaranhados tau, como o semorinemabe e o bepranemabe, da Roche, e as outras duas variações da Biogen. “Existe uma relação muito mais direta entre a presença dessas proteínas no cérebro e as alterações clínicas que afetam os pacientes”, observa. “Se houver um depósito dessa proteína no córtex visual, por exemplo, a pessoa terá problemas nessa função durante a doença de Alzheimer.”
Agora, e se toda a lógica em torno da qual esses medicamentos orbitam - a “cascata amiloide” - naufragar? O que acontece? Aliás, isso é possível? Impossível não é. Muitos especialistas questionam a tese há tempos. Para esse grupo, o acúmulo de placas e emaranhados pode não ser uma causa da doença, mas sua consequência. “Toda teoria científica tem um conteúdo de verdade, mas provavelmente não é inteiramente verdadeira”, pondera Nitrini. “Ela só é científica se puder ser contestada. Assim, vai sendo aprimorada com o tempo. Se isso não acontecer, não é uma teoria, mas um dogma. A hipótese da ‘cascata amiloide’ provavelmente está correta, ainda que ofereça grandes desafios.”
Outro tema inerente às novas drogas é que elas vão exigir diagnósticos que identifiquem os biomarcadores (amiloide e tau) para definir quais pacientes podem ser submetidos aos tratamentos. Hoje, esse tipo de exame é feito por meio de imagens, em tomografias por emissão de prótons (PET), ou pela coleta do líquor, o Líquido Cefalorraqueano (LCR), ou “líquido da espinha”, um fluido corporal produzido pelo cérebro.
Os PETs são caros e raros. “Custam cerca de R$ 6 mil”, diz Bertolucci, da Unifesp. Nitrini, da USP, acrescenta que nem existem PETs para tau no Brasil. No caso do líquor, observa Bertolucci, o valor cai para R$ 2 mil, o que não é pouco, mas os testes têm cobertura dos planos de saúde. O problema é que são invasivos, pois feitos por uma punção lombar.
O melhor seria, apontam os pesquisadores, se houvesse uma alternativa. E como inovações parecem atrair inovações, avança em todo o mundo a pesquisa para obter esse tipo de diagnóstico por meio do sangue - o que seria muito mais fácil e barato. Tecnicamente, contudo, essa não é uma solução trivial.
O sangue é formado por uma maçaroca de proteínas, um caldo no qual é difícil distinguir quem é quem - o que compromete a identificação das supostas vilãs do Alzheimer. Mesmo assim, um teste desse tipo está disponível para médicos nos EUA desde 2020. Ele é comercializado pela C2N Diagnostics, uma empresa com sede em St. Louis, no Missouri. Outra versão do exame foi desenvolvida por uma equipe da Universidade de Ciência e Tecnologia de Hong Kong. Grandes indústrias, como a Roche e a Lilly, também estão concentradas nessa busca.
O aprimoramento dos diagnósticos também pode levar à identificação precoce da doença. Essa é uma janela especialmente oportuna que se abre em relação à enfermidade. Como todas as doenças degenerativas, o Alzheimer é resultado da lenta e constante ação no tempo. Estudos apontam que os níveis de beta-amiloide no cérebro aumentam 22 anos antes do aparecimento dos primeiros sintomas (como a perda de memória de fatos recentes, a desorientação no tempo e no espaço e alterações de comportamento). Ou seja, isso indica que há um período de tempo longo no qual seria possível agir, mas por enquanto nada é feito.
Avanços ocorrem ainda em outras searas da pesquisa sobre o Alzheimer. Na avaliação dos cientistas, terapias que dispensam fármacos, por exemplo, têm obtido resultados impressionantes. Em geral, elas operam a partir da constatação de que a idade avançada é um dos grandes fatores de risco da doença. A enfermidade acomete 5,3% das pessoas entre 65 e 74 anos. Depois disso, esse percentual mais do que dobra, atingindo 13,8% entre os que têm de 75 a 84 anos. Por fim, chega a 34,6% em se tratando de pessoas acima de 85 anos. Sendo que não há como evitar o envelhecimento, o pulo do gato dessas terapias é intervir na forma como as pessoas envelhecem.
A julgar por um relatório publicado em dois tempos pela revista britânica “The Lancet”, especializada em medicina, essa é uma ideia para lá de promissora. Na última versão do documento, de 2020, foram listados 12 fatores de risco entre sociais, de saúde e comportamentais que, se controlados, podem atrasar ou prevenir 40% dos casos de demência. O estudo foi redigido por um grupo de 28 especialistas.
Os temas elencados foram a hipertensão, a baixa escolaridade na infância (a educação é considerada um elemento “protetor” contra o Alzheimer), a deficiência auditiva, o tabagismo, a obesidade, a depressão, o diabetes, o contato social restrito e a inatividade física. Juntos, esses nove elementos estão associados a 34% dos episódios de demência. Já o consumo excessivo de álcool, a poluição do ar e lesões cerebrais traumáticas representam, respectivamente, 1%, 2% e 3% dos casos.
Há outras pesquisas que dão respaldo à tese exposta pela revista britânica. Uma delas foi conduzida pelos brasileiros Sergio Teixeira Ferreira e Fernanda De Feliche, ambos ligados à Universidade Federal do Rio de Janeiro (UFRJ). O trabalho foi publicado em janeiro de 2019 na revista “Nature Medicine”. Ele mostrou que o hormônio irisina, produzido no músculo e liberado pelo corpo durante a atividade física, é importante para a formação de memória e para a proteção de neurônios contra os efeitos tóxicos das vilãs do Alzheimer. Algo que casa perfeitamente com o fator de risco “inatividade física”.
Até aqui, os testes foram feitos em animais geneticamente modificados para desenvolver a doença. “Em linhas gerais, constatamos que a memória dos camundongos que são exercitados é totalmente recuperada”, diz Ferreira. Óbvio, ressalta o pesquisador, que o cérebro humano é muito mais complexo do que o de um rato. “Ainda assim, esse e outros trabalhos que vão na mesma direção nos permitem pensar em prevenção”, frisa. “E essa é uma perspectiva importante no caso do Alzheimer.”
É isso o que indica outro estudo recente, este produzido pela Universidade Harvard e publicado no “Neurology Journal”, da Academia Americana de Neurologia. O levantamento constatou que a taxa real de demência (não só Alzheimer, portanto) nos EUA e na Europa vem diminuindo 13% a cada década ao longo dos últimos 30 anos. Como isso acontece? Na ausência de uma resposta peremptória, eis a hipótese: “O declínio seria resultado de esforços preventivos envolvendo a educação, o estilo de vida e intervenções de saúde”, apontam os cientistas da universidade americana.
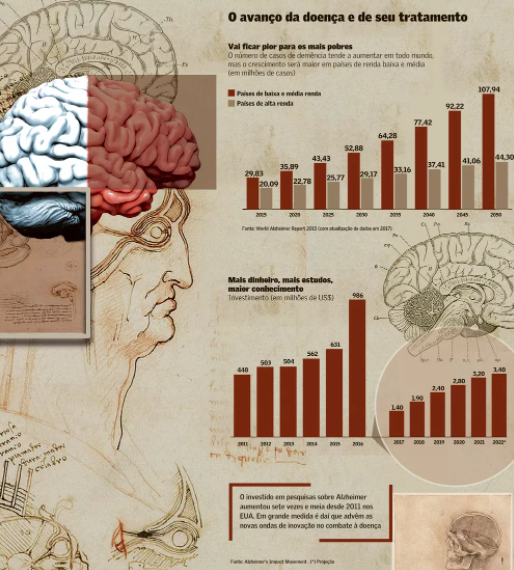
Prevenção, notam os neurologistas, é algo crucial para países de baixa e média renda. Estimativas apontam que 49,9 milhões de pessoas apresentavam algum tipo de demência em 2015 (veja quadro à pág. 9). Desses, 60% viviam em países pobres ou em desenvolvimento. A projeção é que, em 2050, o total de pessoas com esse problema chegue a 152,3 milhões, o equivalente à população da Rússia, sendo que 70% deles estarão vivendo nas regiões entre as mais carentes do globo.
É crescente ainda o número de pesquisadores que lida na interseção entre fatores de risco e medicamentos. Um deles é o médico americano Dale Bredesen, o autor do best-seller “O fim do Alzheimer”, e seu filhote, “O fim do Alzheimer, um guia prático”, ambos editados no Brasil pela Objetiva.
Bredesen desenvolveu um protocolo que batizou de ReCODE, acrônimo para “reversal of cognitive decline” (reversão do declínio cognitivo). Nele, são mapeados 36 fatores metabólicos que podem levar ao desenvolvimento da doença. Seriam equivalentes a fatores de risco. Nos livros, ele narra como o manejo dessas mais de três dezenas de variantes pode até reverter o declínio cognitivo em alguns casos.
O médico é um crítico da visão “monotemática” da “cascata de amiloide”. No geral, contudo, define-se como um otimista em relação ao cenário atual, com o início de “abordagens multifacetadas”. “Os melhores resultados dos trabalhos com pacientes vieram de protocolos de medicina de precisão”, diz. “E os maiores avanços da pesquisa surgiram com a inteligência artificial, a partir da análise de grandes conjuntos de dados.”
Para o pesquisador, a união dessas forças é imprescindível para o combate à doença. “O Alzheimer não é uma consequência de proteínas mal dobradas”, anota. “É a insuficiência de uma rede. Por isso, é importante identificar e direcionar todos os pontos de falha para cada paciente.” Otimista, Bredesen crê que chegou a hora de transformar o Alzheimer em uma “doença rara”. E crava: “Pela primeira vez, isso é possível”.
As soluções nesse sentido, como se viu aqui, não são mirabolantes. Elas são feitas de passos, uns curtos, outros maiores. Some-se a isso o aumento crescente de recursos injetados em estudos sobre a demência. Apenas nos Institutos Nacionais de Saúde (NIH, na sigla em inglês), o conglomerado que forma a agência de pesquisa biomédica do governo americano, essa quantia partiu dos US$ 448 milhões, em 2011, no governo Obama, e deve chegar a US$ 3,2 bilhões, em 2022.
Por enquanto, é esse o conjunto de iniciativas que se propõe a alterar o quadro de Nala, a mulher citada no início desta reportagem, que manteve a habilidade de tocar piano, apesar do severo declínio cognitivo. O caso não chega a ser incomum. Algo semelhante acontece com o cantor Tony Bennett. Ele foi diagnosticado com Alzheimer, mas manteve o domínio sobre o repertório. Bredesen explica: “O que quer que as pessoas tenham feito por muitos anos, como tocar piano ou cantar, tendem a ser as últimas coisas a serem perdidas, já que a repetição expande as partes do cérebro dedicadas a esse esforço. No entanto, e em última análise, o processo degenerativo leva até essas atividades”. É para evitar isso que a ciência tem se movimentado como poucas vezes se viu nesse campo.
Participe também: Grupo de WhatsApp e Telegram para receber notícias farmacêuticas
Obrigado por apoiar o jornalismo profissional






